研究・開発の窓 COLUMN
トランスポーター研究から、新規病型分類提唱や薬物相互作用機序解明へと展開
東京大学医学部附属病院 教授・薬剤部長
高田龍平氏
エゼチミブとワルファリンの薬物相互作用機序を解明
 東京大学医学部附属病院の教授・薬剤部長である高田龍平氏は、薬学の一分野としての「医療薬科学」を掲げ、薬物動態学をベースに医療現場や創薬に還元できる研究を続ける研究者だ。
東京大学医学部附属病院の教授・薬剤部長である高田龍平氏は、薬学の一分野としての「医療薬科学」を掲げ、薬物動態学をベースに医療現場や創薬に還元できる研究を続ける研究者だ。
「医療現場で役立つことだけでなく、scienceも重視するという意味で、『医療薬科学』という言葉を使っている。特に臨床の検体やデータを使った研究と動物や細胞を使った基礎研究を組み合わせた複合的な研究に力を入れ、主に生活習慣病関連栄養物質のトランスポーターによる体内動態制御をテーマとした研究を続けてきた」と高田氏は述べる。
高田氏の代表的な研究の1つが、小腸におけるビタミンK吸収トランスポーターの発見と薬物相互作用の機序解明だ。コレステロール吸収阻害薬エゼチミブにはワルファリン等のクマリン系抗凝血薬との薬物相互作用がある。相互作用の存在は、当初から添付文書に記載されていたが、「機序不明」となっていた。
「エゼチミブはNPC1L1トランスポーターの阻害薬なので、私たちなら謎に迫れるのではないか」と考えた高田氏は、エゼチミブのインタビューフォームに同薬が小腸からのビタミンA、ビタミンDの吸収に影響を及ぼさないと記載されていることに着目した。脂溶性ビタミンにはビタミンEとビタミンKもある。高田氏らは細胞と動物の実験によってNPC1L1トランスポーターからのビタミンE吸収実験を行った。その結果、「NPC1L1トランスポーターは、小腸からのコレステロール吸収だけでなくビタミンEの吸収も担うこと、エゼチミブはその両方を阻害することが分かった」と高田氏。
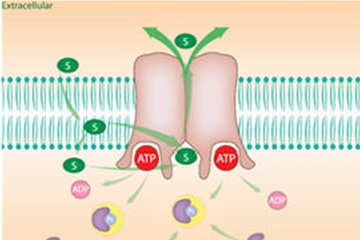
次に高田氏らは同様の実験でNPC1L1トランスポーターがビタミンKを吸収するのかを確かめた。その結果、「小腸からのビタミンK吸収の大部分はNPC1L1トランスポーターを介したものであり、エゼチミブはビタミンKの吸収を阻害することが分かった」と明言。その上で、「ワルファリンは肝臓でのビタミンKサイクルを阻害することで抗凝血作用を発揮するが、エゼチミブと併用するとビタミンKが吸収阻害されて生体内の量が少なくなり、抗凝血作用が増強されてしまう」と薬物相互作用の機序を説明する(図1)。
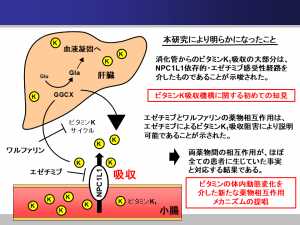
この研究はビタミンK吸収機構に関する初めての知見であり、ビタミンの体内動態変化を介した新たな薬物相互作用メカニズムを提唱したという点でも画期的なものだった。現在では「動脈硬化性疾患予防ガイドライン」にもこの機序が記載されている。
ABCG2トランスポーターが尿酸輸送機能を有することを発見
もう1つの代表的研究は、尿酸トランスポーターABCG2の発見と、それに続く痛風、高尿酸血症の遺伝リスク解明、新たな病型分類提唱につながった研究だ。
プリン体代謝で生成された尿酸は主に腎臓で排出と再吸収を繰り返して、尿中に排泄される。尿酸を腎尿細管管腔側から血管側に再吸収するトランスポーターとしてURAT1、GLUT9があることは、2000年代に日本の研究グループが明らかにしていた。一方、血管側から管腔側に尿酸を排泄するトランスポーターがあることも推測されていたが、具体的には同定されていなかった。
高田氏を含む、東大・防衛医大・東京薬科大の研究グループが着目したのは、多数の薬物の輸送に関与するトランスポーターとして有名なABCG2(BCRP)だ。ABCトランスポーターファミリーはATPを加水分解するエネルギーによって物質を細胞外に輸送する。高田氏らがABCG2トランスポーターによる尿酸排泄を実験してみると、ATP依存的に尿酸が細胞外方向に輸送されることがはっきりと示された。また、尿酸排泄能力には個人差が大きいことが想定されたため、高田氏らは健常者と痛風患者のABCG2遺伝子の大規模解析を行った。
その結果、日本人で頻度の高いSNPが複数見つかった。それぞれのSNPタイプ別にABCG2トランスポーターの尿酸輸送量を調べると、野生型ではATPが存在すると尿酸輸送量が大きく上がるが、Q126Xの変異型ではATPが存在しても尿酸輸送活性はほとんど上昇せず、Q141Kの変異型では野生型の半分程度しか上昇しなかった。
高田氏は「この研究によって、日本人ではABCG2遺伝子の2つのSNPを調べれば、ABCG2トランスポーターによる尿酸排泄能が正常、75%、50%、25%、全く機能が無いの5群に分けることが可能になった」と話す。また、同研究における健常者群(尿酸値7.0 mg/dL以下)では50%以上の被験者のSNPが両方とも野生型だったが、痛風患者群では約80%が変異型を含んでおり、特に、約10%は尿酸排泄能が4分の1(25%)以下しかないことが分かった。ABCG2遺伝子多型解析は大手検査会社によって実用化され、「一部の医療機関でハイリスク患者への食事や服薬の指導に活用されるようになっている」という。
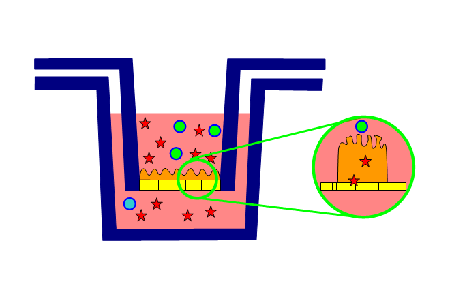
実は、尿酸の排泄ルートは腎からの尿排泄だけではなく、消化管排泄もあることが、以前から指摘されていた。そこで高田氏らはABCG2トランスポーターによる尿酸排泄ルートについての研究を行うことにした。ABCG2ノックアウトマウスを作成し、消化管からの尿酸排泄量を調べると、野生型マウスよりも大きく下がっていた。一方、腎からの尿酸排出量は野生型マウスもABCG2ノックアウトマウスもほとんど差がなかった。このことから、高田氏らは「ABCG2トランスポーターによる尿酸排泄の大部分は消化管で行われる」と結論付けた。
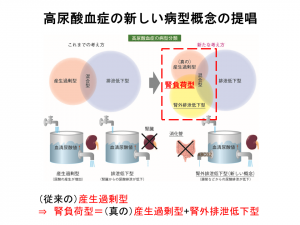
当時、高尿酸血症の病型は尿酸が過剰に生成される「尿酸産生過剰型」と、腎からの排泄が低下する「尿酸排泄低下型」に分類されていた。高田氏らはABCG2トランスポーターによる尿酸排泄ルートの研究成果をもとに、従来の「尿酸産生過剰型」を「(真の)産生過剰型」と「腎外排泄低下型」に分類する新たな病型概念を提唱(図2)。今では「高尿酸血症・痛風の治療ガイドライン」にも記載されている。
高田氏は尿酸トランスポーターと薬物相互作用の研究も行った。2つの尿酸トランスポーター、ABCG2とURAT1に影響する薬剤を網羅的に調べてみると、フェブキソスタットがABCG2を強く阻害することが分かった。単剤使用ではあまり問題は生じていないように見えるが、ABCG2は薬物トランスポーターでもあるため、ABCG2基質薬と併用すると相互作用が生じる可能性がある。ロスバスタチンの単剤投与での消化管吸収に対するABCG2トランスポーターSNPの影響を調べた過去の報告によると、ABCG2の尿酸排泄機能50%のグループではロスバスタチンの血中濃度が100%のグループの2倍程度に上昇していた。フェブキソスタットとの併用でも同じことが起きる可能性があると示唆された。
高田氏らがこの研究成果を論文発表すると、海外の研究グループはロスバスタチンとフェブキソスタットとの併用に関する臨床研究を行い、両剤の併用で明確なロスバスタチンの血中濃度上昇が起きるという結果を発表した。これらのエビデンスが揃ったため、今日では両薬の添付文書に「併用注意」と記載されるようになった。
最近では、尿酸トランスポーターURAT1の阻害薬によるニコチン酸輸送動態の変化、それによる腎保護作用発現の可能性を探る研究も進めている。
高田氏は「尿酸の体内動態はまだ謎が多く、関連するトランスポーターが不明な部分もある。地道にトランスポーターを探す旅を続けるとともに、研究能力を身に付けた臨床薬剤師の育成に力を注ぐ」と話している。
過去の記事
-
皮膚角層は顆粒層SG1細胞の特殊な細胞死「コルネオトーシス」を起点に形成される

東京工科大学 応用生物学部 教授 松井毅氏 -
4月に日本初の「コスメ学環」誕生、佐賀発の化粧品開発・人材創出拠点に

佐賀大学大学院理工学研究科 化粧品科学講座
教授 徳留嘉寛氏 -
薬物の代謝速度や相互作用に関与する小胞体膜トランスポーターの機能を解明する

名古屋市立大学大学院 薬学研究科 教授
荒川大氏 -
消化管全体の生理環境と薬物動態を考慮した革新的な薬物吸収性予測モデルを開発する

昭和薬科大学 薬学部 教授 白坂善之氏
(薬剤学研究室) -
プロテオーム解析を起点に老化関連疾患の病態機序や健康長寿の因子を探索

東京都健康長寿医療センター研究所 研究部長 三浦ゆり氏(老化機構研究チーム プロテオーム研究)